
市場概要
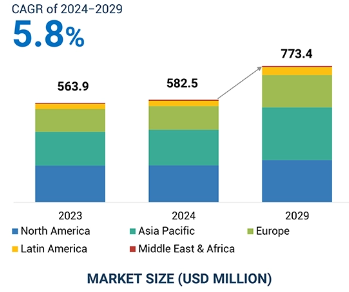
世界の潜在性結核検査市場は、2024年の5億8,250万米ドルから2029年には7億7,340万米ドルに成長し、年平均成長率は5.8%になると予測されています。この市場を牽引する主な要因は、特に免疫不全患者や結核罹患率の高い地域のような高リスク集団における潜在性結核の有病率の上昇です。早期診断に対する意識の高まりや結核対策プログラムの必要性も、インターフェロンγ放出測定法(IGRA)のような信頼性の高い検査法に対する需要を裏付けています。これらの要因はすべて、さまざまな政府機関や国際保健機関、基金による投資の増加によってさらに強化されています。結核撲滅に対するこれらの機関のコミットメントは、高度な診断ツールの開発を促進し、そのような検査へのアクセスを増加させることにより、潜在性結核検査市場に大きな影響を与えています。このため、潜在性結核検査市場は今後数年にわたって安定した成長を続けると予想されます。
潜在性結核感染症(LTBI)は、公衆衛生における最大の課題の1つとして浮上しています。新たに結核を発病した患者のほとんどがLTBI患者であるため、潜在性結核感染の検出と治療は公衆衛生にとって非常に重要です。また、主にHIVなどの感染症に起因する免疫不全者の増加により、潜伏感染から活動性結核に移行するリスクも高まっています。活動性結核の増加傾向は、結核との世界的な闘い、そして最終的な撲滅に向けた重要なステップである、適切なスクリーニングと早期治療を求めています。その結果、公衆衛生上のイニシアチブは、潜伏性結核感染症例の進行を防ぐため、より多くの症例の治療を目標としています。潜在性結核検査は非常に需要が高く、結核制圧に向けた世界的な取り組みにおいて最も重要な焦点の一つとなっています。
償還政策は、潜在性結核検査市場の成長を妨げる重要な要因の一つです。ほとんどの診断企業は、公的・民間どちらの保険会社からも好意的な保険適用を受けることが難しいため、検査の商業化を進めることが困難であると考えています。例えば、一部の診断検査が一般的なコードや未掲載のコードを使用する代わりに特定のコード体系を持たない場合、償還が危うくなります。このような場合、地域の保健当局や保険管理者が償還率を設定するような、調整されていない償還制度になる可能性が高いです。さらに、いくつかの国では診療報酬制度が変更され、一部の検査が低報酬に直面しているため、臨床検査室へのプレッシャーが高まっています。地域によっては、過去数十年にわたり診断検査の報酬が大幅に引き下げられたところもあり、医療制度における予算上の制約が、新しい診断技術の採用におけるさらなる問題となっています。そのため、経済的な障壁が先進的な潜在性結核検査の採用を抑制し続け、市場の成長を鈍らせ、より良い診断法への患者アクセスを遅らせています。企業や医療提供者は、このような複雑な償還環境を乗り切らなければならず、これが世界の潜在性結核検査市場の大きな阻害要因になると予想されます。
インド、ブラジル、トルコ、ロシア、南アフリカのような新興市場は、潜在性結核検査市場の主要プレーヤーに成長機会を提供する可能性があります。その理由は、結核の有病率の高さ、患者数の多さ、医療インフラの整備、可処分所得の増加などの要因によるものです。上記の要因に加え、アジア太平洋地域は、規制やデータ要件が比較的緩やかで、適応力がありビジネスに適したハブとなっています。新興市場におけるヘルスケアおよびライフサイエンス研究への高額投資によって、これらの国々の検査インフラが向上していることがよく表れています。その結果、検査室における診断システムの確立が支援され、高度な診断技術の使用が増加しています。
さらに、発展途上国における早期診断の必要性に対する意識の高まりは、潜在性結核検査キットおよび機器の需要を刺激します。これらの国々では高齢者人口の増加や医療支出の増加が見られ、疾病の早期診断の重要性に対する意識の高まりと相まって、潜在性結核測定キットおよび機器の需要がさらに高まるでしょう。
主要市場の臨床検査室は、変化する状況に適応するため、大規模な運営上の課題に直面しています。特に、潜在性結核のIGRAのような新しい技術が統合されると、検体の収集、保管、輸送が技術者にとって困難になります。したがって、特定の診断検査では、交差汚染のリスクを最小限に抑え、プロセスの効率を高めるために、検査室のセットアップを再設計する必要があります。このような偶発的な変更は、エンドユーザーがハイエンドの診断機器を使用することに集中するため、特に1種類のサンプル用にのみ設計されている場合、運用コストを増加させる可能性があります。さらに、伝染病が頻繁に発生するため、検査室はサンプルの迅速で正確な診断をサポートできる最先端技術の導入を余儀なくされています。しかし、このような技術の進歩は、そのような高度な診断ツールを操作する訓練を受けた熟練技術者の深刻な不足という形で、本質的な課題を突きつけています。このような技術不足は、医療従事者が新しい診断手法を効果的に使用するスキルを備えていない新興市場で最も顕著に見られます。したがって、こうした運用上の障壁や労働力の限界は、革新的な診断ソリューションの統合に影響を及ぼし、この市場の成長にとっての課題となっています。
潜在性結核検査市場は複雑なエコシステムで成り立っています。この市場には、診断ラボ、病院、研究機関が使用するTSTやIGRAなどの検査タイプが含まれます。メーカーは検査の設計と最適化に注力しています。販売業者には、サードパーティ・ベンダーやeコマース・プラットフォームが含まれます。主なステークホルダーは、診断対象となるハイリスク集団、投資家、規制機関などです。
潜在性結核検査市場は、検査の種類によってツベルクリン皮膚テスト(TST)とインターフェロンγ放出測定法(IGRA)に区分できます。2023年の潜在性結核検査市場では、インターフェロンγ放出測定法(IGRA)分野が最も高い市場シェアを獲得しました。IGRA検査はツベルクリン皮膚検査よりも高い特異度と感度を示します。この精度の高さは、すでに結核に感染している人や免疫力が低下している人の間で特に重要であり、より良い治療のためには正しい診断が必要です。IGRA検査のもう1つの利点は、TSTの場合、結果を読み取るために再診が必要なのに比べ、採血のために患者が1回訪れるだけで済むことです。この快適さは、患者のコンプライアンス向上を意味し、全体として、医療提供者にとってプロセスが容易になります。
潜在性結核検査市場は、診断ラボ、病院・診療所、学術・研究機関、その他のエンドユーザーに分類されます。2023年の潜在性結核検査市場で最大の市場シェアを占めたのは診断ラボです。これらの検査機関は、潜在性結核を診断し活動性結核への進行を予防するために、IGRAやTSTを含む様々な検査を実施するための高度な技術と十分な訓練を受けた人材を有しています。世界的に結核の有病率が高まるにつれ、検査を受ける患者の数も増え、診断ラボは医療提供者のネットワークにおいて重要な役割を果たすようになっています。さらに、検査技術の進歩や検査所要時間の短縮の必要性により、医療提供者は主に診断ラボに依存しています。これらの要因が相まって、診断ラボが最大のエンドユーザーセグメントとして脚光を浴びています。
潜在性結核検査市場は、5つの主要地域に区分されています: 北米、欧州、アジア太平洋、中南米、中東・アフリカ。2023年には北米が市場の最前線に。これは、免疫系が低下している人、結核患者と直接接触する人、移民、医療従事者など、一部の層で潜在性結核の症例が増加しているためです。先進的な検査技術がこの地域で広く導入されているのは、優れた診断ラボや、タイムリーで正確な診断のための医療サービスへの幅広いアクセスを有する、確立された高度な医療インフラのためです。研究開発への多額の投資により、北米は結核検査手法の革新に基づく診断の進歩において先行しています。規制の枠組みが強化されたことで、検査サービスがより利用しやすくなり、価格も手頃になったため、医療従事者は新しい優れた技術を受け入れるようになりました。結核の制御と予防に関する公衆衛生プログラムは、結核の早期発見と治療に対する意識の高まりとともに、北米地域における潜在性結核検査に貢献しています。
2024年3月、QIAGEN(オランダ)は国際パネル医師協会(IPPA)との提携を発表し、IGRA要件とそれに関連する患者および医療従事者のメリットに特に焦点を当てながら、最新の結核スクリーニング要件について世界中のパネル医師を支援し、教育しています。
2023年2月、QIAGEN社(オランダ)の結核血液検査QuantiFERON-TB Gold Plusが、98/79/EC体外診断用医療機器指令(IVDD)に代わるEUの体外診断用医療機器規則(IVDR)2017/746に基づくCEマークを取得。
2022年9月、Revvity(Oxford Immunotec)社(米国)は、T-Cell Select試薬キットを使用したT-SPOT.TB検査ワークフローの自動化について、認定ラボによる体外診断用医薬品として米国FDAの承認を取得しました。この試薬キットは、より自動化されたワークフローを可能にし、ラボ担当者の作業時間を短縮し、全体的なコストを削減するように設計されています。
2021年11月、QIAGEN(オランダ)とDiaSorin S.p.A.(イタリア)は、DiaSorinの自動化されたLIAISON XSプラットフォームで使用するLIAISON QuantiFERON-TB Gold Plusアッセイの米国FDA承認を発表しました。この承認により、米国の顧客はQIAGEN社の潜伏結核検出用血液ベース検査の自動化ソリューションへのアクセスが広がりました。
主要企業・市場シェア
潜在性結核検査市場の主要企業は以下の通りです
QIAGEN (Netherlands),
Revvity (US)
Beijing Wantai Biopharmaceutical Co., Ltd. (China)
Sanofi (France)
Endo, Inc. (US)
【目次】
5.1 はじめに
5.2 市場動向 DRIVERS- 潜在性結核の罹患率の増加- BCGワクチンの普及- 結核対策プログラムへの資金援助と助成金の増加 RESTRAINTS- 不利な償還シナリオ OPPORTUNITIES- 新興国における成長機会 CHALLENGES- 規制状況の変化- オペレーションの障壁と労働力不足
5.3 価格分析 製品別平均販売価格 地域別イグラテスト指標価格
5.4 特許分析 主要特許のリスト
5.5 バリューチェーン分析
5.6 サプライチェーン分析
5.7 貿易分析 輸入データ 輸出データ
5.8 エコシステム分析 エコシステムにおける役割
5.9 ポーターの5つの力分析 新規参入の脅威 代替品の脅威 買い手の交渉力 サプライヤーの交渉力 競争相手の強さ
5.10 主要ステークホルダーと購買基準 購買プロセスにおける主要ステークホルダー 主要購買基準
5.11 規制分析 規制ランドスケープ- 北米- 欧州- アジア太平洋- 中南米- 中東 規制機関、政府機関、その他の組織- 北米- 欧州- アジア太平洋- 中南米- その他の地域
5.12 技術分析 主要技術- ツベルクリン皮膚テスト 主要技術- インターフェロンガンマ放出アッセイ
5.13 主要会議とイベント(2024-2025年
5.14 顧客のビジネスに影響を与えるトレンド/混乱
5.15 投資と資金調達のシナリオ
5.16 ケーススタディ分析 ケーススタディ1:LTBI治療のモニタリングにおけるサイトカインの使用法の探求 ケーススタディ2:LTBI検出のためのESAT6-CFP10(EC)皮膚テストの診断精度の評価 ケーススタディ3:HEU乳幼児におけるLTBI検出強化のための白癬菌特異的サイトカイン反応の評価
5.17 主要国の潜伏結核対策 北米- 米国- カナダ 欧州- ドイツ- 英国 アジア太平洋- 日本- 中国- インド- シンガポール
5.18 潜在性結核検査市場におけるAIの主な使用例への影響
潜在性TB検査市場、検査タイプ別
6.1 導入
6.2 高い特異性と精度が市場セグメントを拡大
6.3 TSTの費用対効果が市場成長を促進
潜在性TB検査市場:用途別
7.1 はじめに
7.2 HIV患者による結核とHIVの重複感染率の上昇が成長を促進
7.3 肺結核患者の家庭内接触者(hhc)/結核患者の家庭内接触者(hhc)に対する定期的なスクリーニングの必要性が市場を押し上げる 7.4 その他の用途
7.4 その他の用途
潜在性結核検査市場、エンドユーザー別
8.1 導入
8.2 診断ラボの充実したインフラと能力が検査法の需要を後押し
8.3 病院・診療所の増加、医療への政府投資がこの分野を後押し
8.4 産学連携の活発化が市場成長を支える学術・研究機関
8.5 その他のエンドユーザー
…
【本レポートのお問い合わせ先】
https://www.marketreport.jp/contact
レポートコード:MD 9207