
市場概要
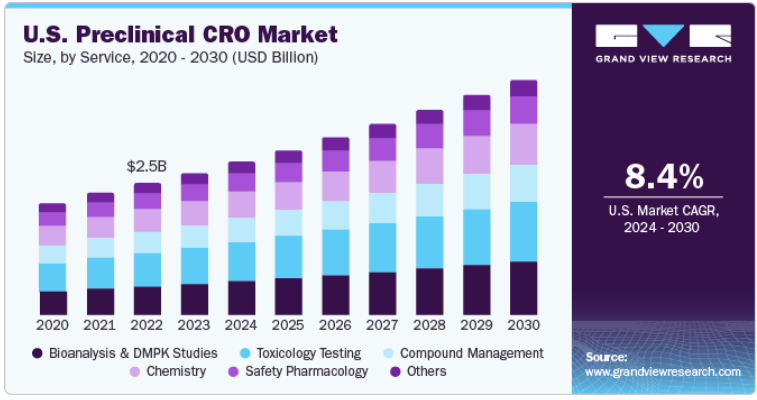
世界の非臨床CRO市場規模は2023年に57.2億米ドルと評価され、2024年から2030年にかけては年平均成長率(CAGR)8.7%で成長すると予測されています。医薬品開発のための研究開発予算の増加により、非臨床試験受託機関(CRO)サービスに対する需要が高まり、予測期間中の市場成長を後押ししています。高分子化合物を扱う前臨床試験の件数の急増と、研究開発費の抑制ニーズの高まりにより、高品質な前臨床 CRO に対する需要の増加が見込まれています。
COVID-19 ワクチンに関しては、前臨床試験が指数関数的なスピードで実施されており、CRO の圧倒的な役割を示しています。CRO サービスへの支出の増加により、予測期間中の市場成長が大幅に促進されると予想されています。また、COVID-19後の医薬品に対する需要の高まりも市場成長にさらに拍車をかけています。世界中のさまざまな組織が、COVID-19後の治療薬や医療機器の開発に多額の資金を提供しています。例えば、米国連邦政府は、2020年のパンデミック発生から2022年3月までの間に、mRNA COVID-19ワクチンに関する研究開発に約23億米ドルを割り当てました。
長年にわたり、米国食品医薬品局(FDA)による医薬品承認プロセスには大きな変化がありました。最近では、画期的な医薬品や医療機器の上市に向けた承認プロセスを迅速化する「21st Century Cures(21世紀治療)法案」が米国で可決されました。こうした承認プロセスの変化はイノベーションを促進すると期待されており、前臨床サービスの需要増加も見込まれ、市場成長に貢献すると考えられています。
さらに、製薬会社の研究開発費の増加とコスト抑制への注力により、CROに対する需要が高まっています。バイオ製薬会社は、製品開発の時間とコストを削減するために、初期開発の研究開発機能をCROにアウトソーシングすることを選択しています。この傾向は、複雑な研究を実施するCROの能力が向上しているため、予測期間中も継続すると予想されます。これにより、ライフサイエンス企業は研究開発費を削減し、コア業務に集中することが可能になります。
世界的な前臨床CRO市場は、新しい技術や手法による高度な革新性を特徴としています。前臨床CRO業界では、創薬および開発技術の絶え間ない進歩が見られます。イメージング、ゲノミクス、その他の分析手法の進歩により、前臨床研究の有効性と精度が向上しています。
LABCORP、Eurofins scientific se.、WuXi AppTec, Inc.、ICON plc などの複数の市場関係者が、合併や買収活動に関与しています。 M&A 活動を通じて、これらの企業は市場での存在感を強化し、新たな地域への進出を拡大することができます。
規制ガイドラインにより、革新的な技術や手法が頻繁に導入されています。市場で優位に立つため、CROは規制要件を満たすか、それを上回る最先端の技術に投資することができます。
主要企業は以下の通りです。 現地の CRO、研究機関、製薬会社とのパートナーシップを構築する。 現地との協力関係は、より円滑な市場参入を促進し、地域の動向に対する理解を深めることができます。
2023年には、非中核の前臨床試験の CRO 研究のアウトソーシングの増加と毒性試験の高い採用率により、毒性試験セグメントが世界の前臨床 CRO 市場の25.4%という最大の収益シェアを占めました。毒性学は、CROによる毒性学試験実施能力の向上により、CROにアウトソーシングされる主要サービスの1つとなっています。 CROへの非中核前臨床試験のアウトソーシングの成長率と、付加価値の高いサービスを提供するCROの能力の向上により、予測期間中のこのセグメントの成長が促進されると予想されます。
バイオアナリシスおよびDMPK研究セグメントは、予測期間中に9.3%という最も速いCAGRを記録すると予測されています。このセグメントは、IND対応研究のための毒性試験をサポートする薬物動態サービスの需要増加により、大きな成長が見込まれています。さらに、バイオアナリシスおよびDMPK研究は、医薬品開発プロセス全体において不可欠です。これらは医薬品開発プロセスのあらゆる段階で実施され、前臨床段階に限定されるものではありません。これらの要因は、セグメントの成長にさらに貢献しています。
患者由来オルガノイド(PDO)モデルセグメントは、2023年に80.6%の最大シェアを占めました。患者由来オルガノイド(PDO)モデルの影響が高まっているのは、患者から直接得られた細胞や組織が使用されているためです。これにより、個別化医療に役立ち、検体を凍結保存することができます。これらの理由により、患者由来オルガノイド(PDO)モデルは、悪性腫瘍のより迅速な診断と予後予測に役立つため、前臨床研究において不可欠な存在になりつつあります。
患者由来異種移植(PDX)モデル市場は、予測期間中に年平均成長率(CAGR)8.4%で成長すると分析されています。これは、患者由来異種移植(PDX)を持つ免疫不全マウスの社内在庫を維持するCROの数が増加していることが要因です。さらに、腫瘍細胞の元々の遺伝的構成が維持されているため、この種の分析により、研究者は研究室での研究と人間との相関関係を導き出すことができます。また、患者を対象とした臨床試験で観察された反応は、これらの患者由来異種移植片における反応と相関関係にあることが判明しており、これにより安全性プロファイルが向上し、新薬調査(NDA)の承認が迅速化されます。
バイオ製薬企業セグメントは、2023年には80.8%の最大市場シェアを占めると予測されています。バイオ製薬企業の間で、特に医薬品開発の前臨床段階で十分な専門知識を持たない中小企業を中心に、エンドツーエンドのサービスをアウトソーシングする傾向が強まっているため、今後は前臨床CROサービスの需要が高まると予想されます。
政府および学術機関セグメントは、予測期間中に9.1%の最も速い成長を遂げると推定されています。学術機関および政府機関は、発見および開発の前臨床段階において重要な役割を果たしています。さらに、前臨床サービスをCROに委託する学術機関および政府機関の増加が、セグメントの成長を後押ししています。学術機関は、Charles River LaboratoriesやLabCorpなどの大手CROの主な収益源の1つです。
主要企業
北米は、Charles River LaboratoriesやLabCorpなどの初期創薬に特化した老舗CROの存在により、2023年には47.2%の最大シェアを占めると予測されています。米国は前臨床試験のアウトソーシング市場としては最大の市場であり、複数のバイオ製薬企業がFDA承認のIND(Investigational New Drug)申請のメリットを享受するために、米国に拠点を置くCROに前臨床試験のアウトソーシングを希望していることが要因となっています。
米国には多数の製薬および生命科学企業が存在するため、前臨床試験のアウトソーシング市場では米国が世界最大のシェアを占めています。米国のCROは、遺伝毒性試験や免疫毒性試験サービスなど、さまざまな能力を備えており、これらのサービスは主に米国で実施されています。これに伴い、個別化医療、希少疾病用医薬品、バイオシミラーなどの新興医療分野の急速な成長が、米国における前臨床試験のアウトソーシング市場の成長を促進することが期待されています。
また、アジア太平洋地域も予測期間中に11.6%という最も速い成長率で成長することが予想されています。多国籍企業のアウトソーシングのビジネスモデルの変化と研究開発費の高騰により、インドや中国などの国々における CRO(医薬品開発業務受託機関)のコスト効率性により、アジア太平洋地域における前臨床試験のアウトソーシングが増加すると予想されています。 西ヨーロッパおよび米国に拠点を置く大手企業は、研究に関連するコストを削減するために、アジア太平洋地域で分析サービス、サイト研究開発、臨床活動を行っています。
日本は世界でも最大規模の医薬品市場のひとつと考えられています。日本の製薬業界の成長は、前臨床試験のアウトソーシングに対する需要の増加につながっています。日本政府が規制面のサポートを提供し、国内での臨床試験を推進する措置を講じているため、国内で実施される臨床試験の数は大幅に増加しています。前臨床試験は開発の中心拠点の近くで実施する必要があるため、これは前臨床試験サービスの市場を刺激するものと見込まれています。
インドの非臨床 CRO:インドの非臨床 CRO 市場は、コスト優位性、熟練した労働力、および好ましい規制環境に後押しされ、著しい成長を遂げています。インドの CRO は競争力のある価格設定を提供しており、非臨床研究のアウトソーシングを求める国際的な製薬会社やバイオテクノロジー企業を引きつけています。インドの非臨床 CRO 市場で事業を展開する主要企業の一部は以下の通りです。
Bioneeds India Private Limited
Jubilant Biosys Ltd. (Jubilant Pharmova Limited Company)
TheraIndx Lifesciences Pvt. Ltd.
Dabur Research Foundation (DRF)
Liveon Biolabs Pvt.Ltd.
Sugen Life Sciences
GVRP
Veeda Clinical Research Limited
前臨床試験受託市場には、大規模な多国籍 CRO と小規模な専門 CRO が存在します。 これには、Labcorp、Charles River Labs、Eurofins Scientific、Intertek Group などが含まれます。 前臨床試験受託市場のシェアは、市場のプレイヤー数、サービスポートフォリオ、治療に関する専門知識、地理的範囲、革新性および投資、さらにはパートナーシップやコラボレーションなど、いくつかの要因によって決まります。例えば、ラボコープの医薬品開発事業であるコヴァンスなどの主要企業は、薬理学および安全性評価、ベクターおよび細胞の特性評価および適格性評価、生体内分布試験およびサービスなど、前臨床試験の包括的なサービス一式を提供しています。また、これらの市場参加者は特定の治療分野や新興分野(例えば、免疫腫瘍学、遺伝子治療)の専門知識も有しています。幅広い地域をカバーしているこれらの企業は、多様な患者集団、規制環境、研究専門知識へのアクセスを顧客に提供することができます。
これにより、主要企業は市場で顕著なシェアを占めることができます。
前臨床 CRO サービスの需要は、製薬およびバイオテクノロジー業界全体の研究開発パイプラインに影響を受けます。創薬および開発への投資の増加は、前臨床研究サービスの需要を促進すると見込まれています。市場力学と競争は、免疫腫瘍学、遺伝子治療、精密医療などの新興治療分野の動向にも影響を受けます。例えば、LabcorpのCovanceは2016年から2020年の間に、世界中で300件以上の前臨床試験と40件以上の細胞・遺伝子治療の臨床試験を実施しました。
主な前臨床試験 CRO企業:
ユーロフィン・サイエンティフィック
PRAヘルス・サイエンシズ
無錫アプテック
メドペース
チャールズ・リバー・ラボラトリーズ・インターナショナル
PPD(サーモフィッシャーサイエンティフィック
SGA SA
Intertek Group Plc (IGP)
LABCORP
Crown Bioscience
2023年3月、Crown Bioscience & JSR Life Sciences Companyは、シンガポールに新たな拠点を設立し、現地およびグローバルなバイオテクノロジーおよび製薬会社の業務拡大を支援すると発表しました。この施設は、前臨床およびトランスレーショナル腫瘍学の創薬および開発に取り組む企業を支援します。
2023年2月、Apax Partnersは、世界的に認められたグローバルCROであるPorsoltを買収しました。この提携により、Porsoltのサービス提供が強化されるとともに、世界中の消費者向けの薬剤スクリーニング、安全性、有効性に関する製品ポートフォリオと能力が拡大します。
このレポートでは、2018年から2030年までの各サブセグメントにおける収益成長の予測と最新動向の分析を提供しています。このレポートでは、Grand View Researchは、サービス、モデルタイプ、エンドユース、地域に基づいて前臨床CRO市場をセグメント化しています。
サービス別展望(収益、10億米ドル、2018年~2030年
バイオアナリシスおよびDMPK研究
インビトロADME
インビボPK
毒性試験
GLP
非GLP
化合物管理
プロセス研究開発
カスタム合成
その他
化学
薬化学
計算化学
安全性薬理学
その他
モデルタイプ別予測(収益、2018年~2030年、単位:10億米ドル)
患者由来オルガノイド(PDO)モデル
患者由来異種移植モデル
エンドユースの展望(収益、2018年~2030年の米ドル十億単位)
バイオ製薬企業
政府および学術機関
医療機器企業
地域別の展望(収益、2018年~2030年の米ドル十億単位)
北米
米国
カナダ
ヨーロッパ
英国
ドイツ
フランス
イタリア
スペイン
スウェーデン
ノルウェー
デンマーク
アジア太平洋
日本
中国
インド
韓国
オーストラリア
タイ
中南米
ブラジル
メキシコ
アルゼンチン
中東およびアフリカ
南アフリカ
サウジアラビア
UAE
クウェート
【目次】
第1章 臨床試験前CRO市場:方法論と範囲
1.1 市場区分と範囲
1.1.1 地域的範囲
1.1.2 予測と予測のタイムライン
1.2 調査方法論
1.3 情報収集
1.3.1 購入データベース
1.3.2 Gvrの内部データベース
1.3.3 二次情報源
1.3.4 一次調査
1.3.5 一次調査の詳細
1.4 情報またはデータ分析
1.4.1 データ分析モデル
1.5 市場の策定および検証
1.6 モデルの詳細
1.6.1 商品フロー分析(モデル1
1.6.2 数量価格分析(モデル2
1.7 二次情報源のリスト
1.8 一次情報源のリスト
1.9 略語のリスト
1.10 目的
1.10.1 目的 – 1
1.10.2 目的 – 2
1.10.3 目的 – 3
1.10.4 目的 – 4
第2章 前臨床CRO市場:エグゼクティブサマリー
2.1 市場の見通し
第3章 前臨床CRO市場:変数、トレンド、および範囲
3.1 セグメントの見通し
3.2 市場力学
3.2.1 市場推進要因分析
3.3 増加する研究開発の海外委託
3.3.1 増加するアウトソーシングの傾向
3.3.2 生命科学企業がコアコンピタンスに集中
3.3.2 市場抑制要因の分析
3.3.2.1 問題の監視と標準化の欠如
3.4 前臨床 CRO 市場分析ツール
3.4.1 ポーターのファイブフォース分析
3.4.2 業界分析 ポーター
3.4.2.1 競合他社との競争(高い
3.4.2.2 買い手の交渉力(高い
3.4.2.3 売り手の交渉力(低い
3.4.2.4 代替品の脅威(低い
3.4.2.5 新規参入の脅威(低い
3.4.3 PESTEL 分析
3.4.3.1 PESTLE 分析
3.4.3.1.1 政治および法律
3.4.3.1.1.1 強み
3.4.3.1.1.2 弱み
3.4.3.1.1.3 機会
3.4.3.1.1.4 脅威
3.4.3.1.2 経済
3.4.3.1.2.1 強み
3.4.3.1.2.2 弱み
3.4.3.1.2.3 機会
3.4.3.1.2.4 脅威
3.4.3.1.3 社会および環境
3.4.3.1.3.1 強み
3.4.3.1.3.2 弱み
3.4.3.1.3.3 機会
3.4.3.1.3.4 脅威
3.5 COVID-19 影響分析
第4章 サービス事業分析
4.1 臨床前CRO市場:サービス動向分析
4.2 バイオアナリシスおよびDMPK研究
4.2.1 バイオアナリシスおよびDMPK研究市場、2018年~2030年(10億米ドル)
4.3 インビトロADME
4.3.1. インビトロADME市場、2018年~2030年(10億米ドル)
4.4. インビボPk
4.4.1. インビボPk市場、2018年~2030年(10億米ドル)
4.5. 毒性試験
4.5.1. 毒性試験市場、2018年~2030年(10億米ドル)
4.5.2. GLP
4.5.2.1. GLP市場、2018年~2030年(10億米ドル)
4.5.3. 非GLP
4.5.3.1. 非GLP市場、2018年~2030年(10億米ドル)
4.6. 化合物管理
4.6.1. 化合物管理企業市場、2018年~2030年(10億米ドル)
4.6.2. プロセス研究開発
4.6.2.1. プロセス研究開発市場、2018年~2030年(単位:10億米ドル)
4.6.3. カスタム合成
4.6.3.1. カスタム合成市場、2018年~2030年(単位:10億米ドル)
4.6.4. その他
4.6.4.1. その他市場、2018年~2030年(10億米ドル)
4.7. 化学
4.7.1. 化学試験市場、2018年~2030年(10億米ドル)
4.7.2. 薬化学
4.7.2.1. 薬化学市場、2018年~2030年(10億米ドル)
4.7.3. 計算化学
4.7.3.1. 計算化学市場、2018年~2030年(10億米ドル)
4.8. 安全性薬理学
4.8.1. 安全性薬理学市場、2018年~2030年(10億米ドル)
4.9. その他
4.9.1. その他市場、2018年~2030年(単位:10億米ドル
第5章 モデルタイプ別ビジネス分析
5.1. 前臨床CRO市場:モデルタイプ別動向分析
5.2. 患者由来オルガノイド(PDO)モデル
5.2.1. 患者由来オルガノイド(PDO)モデル市場、2018年~2030年(単位:10億米ドル)
5.3. 患者由来異種移植(PDX)モデル
5.3.1. 患者由来異種移植(PDX)モデル市場、2018年~2030年(10億米ドル)
第6章 エンドユース別ビジネス分析
6.1. 前臨床CRO市場:エンドユース別動向分析
6.2. バイオ製薬企業
6.2.1. バイオ製薬企業市場、2018年~2030年(単位:10億米ドル
6.3. 政府および学術機関
6.3.1. 政府および学術機関のバリデーション市場、2018年~2030年(単位:10億米ドル
6.4. 医療機器企業
6.4.1. 医療機器企業市場、2018年~2030年(単位:10億米ドル)
第7章 地域別ビジネス分析
7.1. 前臨床CRO市場シェア、地域別、2023年および2030年
7.2. 北米
7.2.1. 北米前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.2.2. 米国
7.2.2.1. 主要国の動向
7.2.2.2. 規制の枠組み
7.2.2.3. 競合状況
7.2.2.4. 米国の前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.2.3. カナダ
7.2.3.1. 主要国の動向
7.2.3.2. 規制の枠組み
7.2.3.3. 競合シナリオ
7.2.3.4. カナダ前臨床CRO市場、2018年~2030年(10億米ドル)
7.3. 欧州
7.3.1. 欧州前臨床CRO市場、2018年~2030年(10億米ドル)
7.3.2. 英国
7.3.2.1. 主要国の動向
7.3.2.2. 競合状況
7.3.2.3. 英国の非臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.3.3. ドイツ
7.3.3.1. 主要国の動向
7.3.3.2. 競合状況
7.3.3.3. ドイツ 前臨床 CRO 市場、2018年~2030年(単位:10億米ドル)
7.3.4. フランス
7.3.4.1. 主要国の動向
7.3.4.2. 競合状況
7.3.4.3. フランス 前臨床 CRO 市場、2018年~2030年(単位:10億米ドル)
7.3.5. イタリア
7.3.5.1. 主要国の動向
7.3.5.2. 競合シナリオ
7.3.5.3. イタリア前臨床CRO市場、2018年~2030年(10億米ドル)
7.3.6. スペイン
7.3.6.1. 主要国の動向
7.3.6.2. 競合シナリオ
7.3.6.3. スペイン前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.3.7. スウェーデン
7.3.7.1. 主要国の動向
7.3.7.2. 競合状況
7.3.7.3. スウェーデン前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.3.8. ノルウェー
7.3.8.1. 主要国のダイナミクス
7.3.8.2. 競合シナリオ
7.3.8.3. ノルウェー前臨床CRO市場、2018年~2030年(10億米ドル)
7.3.9. デンマーク
7.3.9.1. 主要国のダイナミクス
7.3.9.2. 競合シナリオ
7.3.9.3. デンマークの前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4. アジア太平洋
7.4.1. アジア太平洋の前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4.2. 日本
7.4.2.1. 主要国の動向
7.4.2.2. 競合状況
7.4.2.3. 日本 前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4.3. 中国
7.4.3.1. 主要国の動向
7.4.3.2. 競合状況
7.4.3.3. 中国 前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4.4. インド
7.4.4.1. 主要国の動向
7.4.4.2. 競合シナリオ
7.4.4.3. インドの非臨床試験受託機関の一覧
7.4.4.4. インドの非臨床試験受託機関市場、2018年~2030年(単位:10億米ドル)
7.4.5. オーストラリア
7.4.5.1. 主要国の動向
7.4.5.2. 競合シナリオ
7.4.5.3. オーストラリア前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4.6. 韓国
7.4.6.1. 主要国の動向
7.4.6.2. 競合状況
7.4.6.3. 韓国前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.4.7. タイ
7.4.7.1. 主要国の動向
7.4.7.2. 競合シナリオ
7.4.7.3. タイの前臨床CRO市場、2018年~2030年(10億米ドル)
7.5. ラテンアメリカ
7.5.1. ラテンアメリカの前臨床CRO市場、2018年~2030年(10億米ドル)
7.5.2. ブラジル
7.5.2.1. 主要国の動向
7.5.2.2. 競合状況
7.5.2.3. ブラジル前臨床CRO市場、2018年~2030年(10億米ドル)
7.5.3. メキシコ
7.5.3.1. 主要国の動向
7.5.3.2. 競合状況
7.5.3.3. メキシコ前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.5.4. アルゼンチン
7.5.4.1. 主要国の動向
7.5.4.2. 競合状況
7.5.4.3. アルゼンチン前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.6. 中東およびアフリカ
7.6.1. 中東・アフリカの前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.6.2. 南アフリカ
7.6.2.1. 主要国の動向
7.6.2.2. 競合状況
7.6.2.3. 南アフリカの前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.6.3. サウジアラビア
7.6.3.1. 主要国の動向
7.6.3.2. 競合状況
7.6.3.3. サウジアラビアの前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.6.4. アラブ首長国連邦
7.6.4.1. 主要国の動向
7.6.4.2. 競合状況
7.6.4.3. アラブ首長国連邦前臨床CRO市場、2018年~2030年(単位:10億米ドル)
7.6.5. クウェート
7.6.5.1. 主要国の動向
7.6.5.2. 競合状況
7.6.5.3. クウェート前臨床CRO市場、2018年~2030年(単位:10億米ドル)
…
【本レポートのお問い合わせ先】
https://www.marketreport.jp/contact
レポートコード:GVR-2-68038-035-4