
市場概要
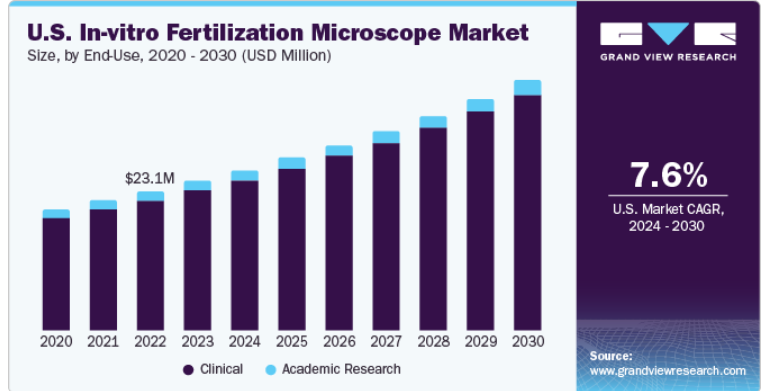
体外受精用顕微鏡の世界市場規模は2023年には1億9780万米ドルと推定され、2024年から2030年までの年間平均成長率(CAGR)は8.45%で成長すると予測されています。体外受精(IVF)の成功率の向上や、経済的支援の拡大といった要因が市場成長の要因となっており、予測期間中の市場拡大が見込まれています。さらに、メーカーによる製品イノベーションは治療効率の向上と処置コストの削減につながり、新たな技術の採用をさらに後押ししています。
過去数年間で、体外受精で使用される顕微鏡および顕微鏡関連機器は著しい進歩を遂げています。研究者らは、プロセスを改善するために、AI、胚評価、精子選択におけるイノベーションの開発に重点的に取り組んでいます。例えば、2022年12月には、ワイル・コーネル・メディシン(Weill Cornell Medicine)の研究者が、体外受精された胚の染色体数が異常か正常かを判断できるAIアルゴリズム「STORK-A」の開発を発表しました。STORK-Aの精度は約70%で、受精後5日目に撮影した胚の顕微鏡画像、クリニックスタッフが胚に割り当てた品質スコア、母親の年齢、そして体外受精のプロセス中に通常収集されるその他のデータを使用します。この非侵襲的な方法は、体外受精の成功率を大幅に改善し、侵襲的な検査の必要性を減らす可能性を秘めています。
さらに、近年、高コントラスト画像技術や関連機器の革新など、顕著な進歩を遂げていることから、体外受精用顕微鏡の採用が増加しています。例えば、2019年に欧州生殖・発生学会(ESHRE)が収集した年間データでは、体外受精(IVF)の実施件数の増加と、それに対応する成功率の向上が明らかになりました。この傾向は、体外受精(IVF)用途における顕微鏡検査の品質向上を継続的に確保するために重要な体外受精(IVF)用顕微鏡のさらなる技術革新を促す取り組みを推進しています。
さらに、体外受精の成功率の高まりにより、この市場に個人投資家が参入し、個人開業/医師所有のビジネスモデルから投資家主導の業界へと移行しました。この産業化により、焦点は体外受精の成果から収益へと移行しました(コモディティ化)。これにより、クリニックのチェーン展開などの活動により、当初は成長が見られましたが、これらのセンターでは徐々に出生率が低下しました。
市場成長段階は中程度で、ペースは加速しています。市場は、体外受精用顕微鏡関連機器における顕微鏡検査の品質向上による高度な技術革新によって特徴づけられます。また、市場は、大手企業によるM&A(合併・買収)活動が活発であることも特徴です。これは、体外受精クリニックにおける高度な顕微鏡製品の採用が、処理時間の短縮と効率性の向上により、患者の体外受精費用削減につながると期待されていることなど、いくつかの要因によるものです。
例えば、2022年7月には、エスコ・ライフサイエンス・グループが体外受精の品質管理システムおよび管理技術を提供するソフトウェア企業、エビデンス・ソリューションの買収を発表しました。エビデンス・ウィットネス・システムは、体外受精クリニックにおけるワークフローのスケジューリング、ラベリング、およびトレーサビリティを可能にし、治療におけるエラーを防止します。
市場は規制当局の監視も強化される傾向にあります。これは体外受精サービスに対する認識が高まっているためで、発展途上国でも規制導入に向けた措置が取られています。この市場で事業を展開する企業は、米国生殖医学会や欧州生殖医学会などの機関が定めたガイドラインに従う必要があります。
地域集中が体外受精顕微鏡の拡大を後押ししており、クリニックの拡大に向けた民間投資家の投資獲得に重点が置かれています。この戦略的フォーカスにより、特定の地理的エリアに合わせた体外受精顕微鏡の有効性が向上します。
用途別では、2023年には臨床セグメントが最大の収益シェア94%を占め、市場をリードしました。このセグメントの成長は、さまざまな国々における施設拡張への投資増加によるものです。例えば、2021年5月には、西アジアに拠点を置くガルフ・キャピタルのART不妊治療クリニックが、2023年までにインドの主要都市に18のクリニックを建設するために3000万米ドルを投資する計画を発表しました。さらに、費用対効果、専門家の確保、卵子・精子バンクとの生産的な関係、院内感染リスクの最小化などの要因も、このセグメントの成長に寄与しています。
体外受精クリニックは、予測期間において最も速いCAGRを記録すると予測されています。体外受精クリニックは、健康な卵子の評価、精液の分析、顕微授精(ICSI)の実施、胚のモニタリング、胚の凍結保存など、さまざまなサービスを提供しています。これらのクリニックは、民間投資家の支援を受け、新しい改良されたサービスを導入しています。
2023年には、ヨーロッパが市場の約38%の収益シェアを占め、市場を支配しました。この地域の成長に貢献した主な要因には、好ましい規制変更と革新的な技術が含まれます。クリニック向けに設計されたアルゴリズムによる時間経過技術の採用が広く普及しており、単一の胚チャンバーで全ての画像要件を提供する顕微鏡の開発により、処置に必要なコストとスペースが削減されています。さらに、LGBTQ+コミュニティへの体外受精へのアクセス提供など、最近の法改正も市場に好影響を与えています。
アジア太平洋地域は、予測期間にわたって大幅なCAGRが見込まれています。この成長は、人口の多さと体外受精に関する認識の高まりによるものです。さらに、不妊治療ツーリズムの成長、経済的に発展途上国への進出を図る国際企業の増加、アジア太平洋地域の規制環境の変化により、体外受精治療の需要が増加すると予想されています。さらに、主要企業が製品コストの削減と現地生産に重点的に取り組むことで、市場成長に貢献することが期待されています。
主要企業・市場シェア
市場で事業を展開する主要企業の一部には、ライカマイクロシステムズ、オリンパス株式会社、ツァイス、および株式会社ニコンが含まれます。
ライカマイクロシステムズは2005年よりダナハーの子会社となり、現在はライフサイエンスおよび診断部門に属しています。同社は顕微鏡および科学機器を製造しており、ライフサイエンス、医療、産業の3つの部門で事業を展開しています
オリンパス株式会社は、4つのセグメントを通じて事業を展開しています。内視鏡ソリューション部門、治療ソリューション部門、科学ソリューション部門、イメージング部門です。同社の科学ソリューション部門では、計測・画像処理機器、顕微鏡、ビデオスコープ、X線分析装置を提供しています。同社は約39カ国で事業を展開しています
Nikon Corporation、Euromex Microscopen BV、Sutter Instrument Companyは、新興市場の参加企業です。
Nikon Corporationは、光学ガラス、イメージング製品、ヘルスケア製品、産業計測製品などの光学機器を製造しています。 同社は、産業計測、ヘルスケア、精密機器、イメージング製品の4つのセグメントで事業を展開しています。 顕微鏡ソリューション部門は、ヘルスケア事業部門の一部です
Sutter Instrument Company は研究用機器のメーカーです。 同社の製品ラインナップには、イメージング製品、顕微鏡、アンプ、マイクロマニピュレーター、ステージ&トランスレーター、灌流システムなどが含まれます。 同社は北米、中南米、ヨーロッパ、アジア、オーストラリア/ニュージーランド、中東の約49か国に広がる代理店ネットワークを通じて、世界中に製品を供給しています
体外受精用顕微鏡の主要企業:
Linkam Scientific Instruments
オリンパス株式会社
ライカマイクロシステムズ(ダナハーコーポレーション)
明治テクノ
ツァイス
ユーロメックスマイクロスコープB.V.
ラボメッド株式会社
株式会社ニコン
ナリシゲグループ
エッペンドルフAG
ハミルトン・ソーン株式会社
サッター・インスツルメント・カンパニー
トリテック・リサーチ株式会社
2023年10月、Hamilton Thorne Ltd.はGynetics Medical ProductsとGynetics Servicesを買収しました。この買収により、Hamilton Thorneは専門知識、製造能力、消耗品(特に急速に成長している欧州の体外受精市場)の製品ラインナップを拡大することができました。
2022年12月、Hamilton Thorne Ltd.は、コンピュータ支援精液分析(CASA)ソフトウェア、消耗品、AIを組み込んだ画像分析システムの開発で業界をリードするMicroptic, S.Lを買収しました。この買収により、体外受精クリニック向けのCASA市場におけるHamilton Thorneの地位が強化されました。
このレポートでは、地域別および国別の収益成長を予測し、2018年から2030年までの各サブセグメントにおける業界の最新動向を分析しています。このレポートでは、Grand View Researchは、体外受精用顕微鏡市場をエンドユースと地域に基づいて区分しています。
エンドユース別予測(収益、米ドル百万、2018年~2030年)
臨床
学術研究
地域別展望(収益、百万米ドル、2018年~2030年)
北米
米国
カナダ
欧州
英国
ドイツ
フランス
イタリア
スペイン
スウェーデン
ノルウェー
デンマーク
アジア太平洋
日本
中国
インド
オーストラリア
タイ
韓国
中南米
ブラジル
メキシコ
アルゼンチン
中東・アフリカ
南アフリカ
サウジアラビア
アラブ首長国連邦
クウェート
【目次】
第1章 体外受精顕微鏡市場:調査手法および範囲
1.1. 市場区分と範囲
1.2. 区分の定義
1.2.1. 用途
1.2.2. 地域的範囲
1.2.3. 予測と見通しのタイムライン
1.3. 調査手法
1.4. 情報収集
1.4.1. 購入データベース
1.4.2. GVRの内部データベース
1.4.3. 二次情報源
1.4.4. 一次調査
1.5. 情報またはデータの分析
1.5.1. データ分析モデル
1.6. 市場の策定と検証
1.7. モデルの詳細
1.7.1. 商品フロー分析(モデル1
1.7.2. 数量価格分析(モデル2
1.8. 二次情報源の一覧
1.9. 一次情報源の一覧
1.10. 目的
第2章 体外受精顕微鏡市場:エグゼクティブサマリー
2.1. 市場スナップショット
2.2. セグメントスナップショット
2.2.1. 用途別見通し
2.2.2. 地域別見通し
2.3. 競合状況スナップショット
第3章 体外受精顕微鏡市場:市場変数、トレンド、および展望
3.1. 市場系譜の展望
3.1.1. 親市場の展望
3.1.2. 関連/補助市場の展望
3.2. 市場力学
3.2.1. 市場推進要因の分析
3.2.1.1. 成功率の向上による普及率の増加
3.2.1.2. 技術の進歩
3.2.2. 市場抑制要因の分析
3.2.2.1. 体外受精ガイドラインによる抑制
3.2.2.2. コモディティ化と工業化
3.3. 体外受精用顕微鏡 市場分析ツール
3.3.1. 業界分析 – ポーターの
3.3.1.1. 供給業者の力
3.3.1.2. 購入業者の力
3.3.1.3. 代替品の脅威
3.3.1.4. 新規参入の脅威
3.3.1.5. 競合の競合
3.3.2. PESTLE分析
第4章 体外受精用顕微鏡市場:用途別分析
4.1. 用途別市場シェア、2023年および2030年
4.2. セグメントダッシュボード
4.3. 体外受精用顕微鏡の世界市場:用途別展望
4.4. 市場規模・予測およびトレンド分析(2018年~2030年)
4.4.1. 臨床
4.4.1.1. 臨床市場、2018年~2030年(百万米ドル
4.4.2. 学術研究
4.4.2.1. 学術研究市場、2018年~2030年(百万米ドル)
第5章 体外受精顕微鏡市場:地域別分析
5.1. 地域別市場シェア分析、2023年および2030年
5.2. 地域別市場ダッシュボード
5.3. 世界の地域別市場の概観
5.4. 市場規模、および予測 傾向分析、2018年から2030年:
5.5. 北米
5.5.1. 米国
5.5.1.1. 主要国の動向
5.5.1.2. 規制のシナリオ
5.5.1.3. 競合のシナリオ
5.5.1.4. 米国体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.5.2. カナダ
5.5.2.1. 主要国の動向
5.5.2.2. 規制シナリオ
5.5.2.3. 競合シナリオ
5.5.2.4. カナダ体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6. 欧州
5.6.1. ドイツ
5.6.1.1. 主要国の動向
5.6.1.2. 規制シナリオ
5.6.1.3. 競合シナリオ
5.6.1.4. ドイツ体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.2. 英国
5.6.2.1. 主要国の動向
5.6.2.2. 規制シナリオ
5.6.2.3. 競合シナリオ
5.6.2.4. 英国体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.3. フランス
5.6.3.1. 主要国の動向
5.6.3.2. 規制シナリオ
5.6.3.3. 競合シナリオ
5.6.3.4. フランス体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.4. イタリア
5.6.4.1. 主要国の動向
5.6.4.2. 規制シナリオ
5.6.4.3. 競合シナリオ
5.6.4.4. イタリア体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.5. スペイン
5.6.5.1. 主要国の動向
5.6.5.2. 規制シナリオ
5.6.5.3. 競合シナリオ
5.6.5.4. スペイン体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.6. スウェーデン
5.6.6.1. 主要国の動向
5.6.6.2. 規制シナリオ
5.6.6.3. 競合シナリオ
5.6.6.4. スウェーデン体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.7. ノルウェー
5.6.7.1. 主要国の動向
5.6.7.2. 規制シナリオ
5.6.7.3. 競合シナリオ
5.6.7.4. ノルウェー体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.6.8. デンマーク
5.6.8.1. 主要国の動向
5.6.8.2. 規制シナリオ
5.6.8.3. 競合シナリオ
5.6.8.4. デンマーク体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.7. アジア太平洋
5.7.1. 日本
5.7.1.1. 主要国の動向
5.7.1.2. 規制シナリオ
5.7.1.3. 競合シナリオ
5.7.1.4. 日本体外受精顕微鏡市場、2018年~2030年(百万米ドル)。
5.7.2. 中国
5.7.2.1. 主要国の動向
5.7.2.2. 規制シナリオ
5.7.2.3. 競合シナリオ
5.7.2.4. 中国体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.7.3. インド
5.7.3.1. 主要国の動向
5.7.3.2. 規制シナリオ
5.7.3.3. 競合シナリオ
5.7.3.4. インド体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.7.4. オーストラリア
5.7.4.1. 主要国の動向
5.7.4.2. 規制シナリオ
5.7.4.3. 競合状況
5.7.4.4. オーストラリア体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.7.5. 韓国
5.7.5.1. 主要国の動向
5.7.5.2. 規制シナリオ
5.7.5.3. 競合シナリオ
5.7.5.4. 韓国体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.7.6. タイ
5.7.6.1. 主要国動向
5.7.6.2. 規制シナリオ
5.7.6.3. 競合シナリオ
5.7.6.4. タイ体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.8. ラテンアメリカ
5.8.1. ブラジル
5.8.1.1. 主要国の動向
5.8.1.2. 規制のシナリオ
5.8.1.3. 競合のシナリオ
5.8.1.4. ブラジル体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.8.2. メキシコ
5.8.2.1. 主要国の動向
5.8.2.2. 規制シナリオ
5.8.2.3. 競合シナリオ
5.8.2.4. メキシコ体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.8.3. アルゼンチン
5.8.3.1. 主要国動向
5.8.3.2. 規制シナリオ
5.8.3.3. 競合状況
5.8.3.4. アルゼンチン体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.9. 中東およびアフリカ
5.9.1. 南アフリカ
5.9.1.1. 主要国の動向
5.9.1.2. 規制状況
5.9.1.3. 競合状況
5.9.1.4. 南アフリカ体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.9.2. サウジアラビア
5.9.2.1. 主要国の動向
5.9.2.2. 規制シナリオ
5.9.2.3. 競合シナリオ
5.9.2.4. サウジアラビア体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.9.3. UAE
5.9.3.1. 主要国の動向
5.9.3.2. 規制シナリオ
5.9.3.3. 競合シナリオ
5.9.3.4. アラブ首長国連邦(UAE)体外受精顕微鏡市場、2018年~2030年(百万米ドル)
5.9.4. クウェート
5.9.4.1. 主要国の動向
5.9.4.2. 規制のシナリオ
5.9.4.3. 競合のシナリオ
5.9.4.4. クウェート体外受精顕微鏡市場、2018年~2030年(百万米ドル)
第6章 競合分析
6.1. 主要市場参加者の最近の動向と影響分析
6.2. 企業/競合の分類
6.3. ベンダーの概観
6.3.1. 主要な代理店とチャネルパートナーの一覧
6.3.2. 主要顧客
6.3.3. 主要企業の市場シェア分析、2023年
6.3.4. Linkam Scientific Instruments
6.3.4.1. 企業概要
6.3.4.2. 財務実績
6.3.4.3. 製品ベンチマーク
6.3.4.4. 戦略的イニシアティブ
6.3.5. Olympus Corporation
6.3.5.1. 企業概要
6.3.5.2. 財務実績
6.3.5.3. 製品ベンチマーキング
6.3.5.4. 戦略的イニシアティブ
6.3.6. ライカマイクロシステムズ
6.3.6.1. 会社概要
6.3.6.2. 財務実績
6.3.6.3. 製品ベンチマーキング
6.3.6.4. 戦略的イニシアティブ
6.3.7. 明治テクノ
6.3.7.1. 会社概要
6.3.7.2. 財務実績
6.3.7.3. 製品ベンチマーク
6.3.7.4. 戦略的イニシアティブ
6.3.8. ZEISS
6.3.8.1. 会社概要
6.3.8.2. 財務実績
6.3.8.3. 製品ベンチマーク
6.3.8.4. 戦略的イニシアティブ
6.3.9. Euromex Microscopen BV
6.3.9.1. 企業概要
6.3.9.2. 財務実績
6.3.9.3. 製品ベンチマーク
6.3.9.4. 戦略的イニシアティブ
6.3.10. Labomed, Inc.
6.3.10.1. 企業概要
6.3.10.2. 財務実績
6.3.10.3. 製品ベンチマーキング
6.3.10.4. 戦略的イニシアティブ
6.3.11. 株式会社ニコン
6.3.11.1. 会社概要
6.3.11.2. 財務実績
6.3.11.3. 製品ベンチマーキング
6.3.11.4. 戦略的イニシアティブ
6.3.12. ナリシゲグループ
6.3.12.1. 会社概要
6.3.12.2. 財務実績
6.3.12.3. 製品ベンチマーク
6.3.12.4. 戦略的イニシアティブ
6.3.13. エッペンドルフ
6.3.13.1. 会社概要
6.3.13.2. 財務実績
6.3.13.3. 製品ベンチマーク
6.3.13.4. 戦略的イニシアティブ
6.3.14. ハミルトン・ソーン社
6.3.14.1. 企業概要
6.3.14.2. 財務実績
6.3.14.3. 製品ベンチマーク
6.3.14.4. 戦略的イニシアティブ
6.3.15. サター・インスツルメント社
6.3.15.1. 企業概要
6.3.15.2. 財務実績
6.3.15.3. 製品ベンチマーキング
6.3.15.4. 戦略的イニシアティブ
6.3.16. Tritech Research, Inc
6.3.16.1. 会社概要
6.3.16.2. 財務実績
6.3.16.3. 製品ベンチマーキング
6.3.16.4. 戦略的イニシアティブ
…
【本レポートのお問い合わせ先】
https://www.marketreport.jp/contact
レポートコード: